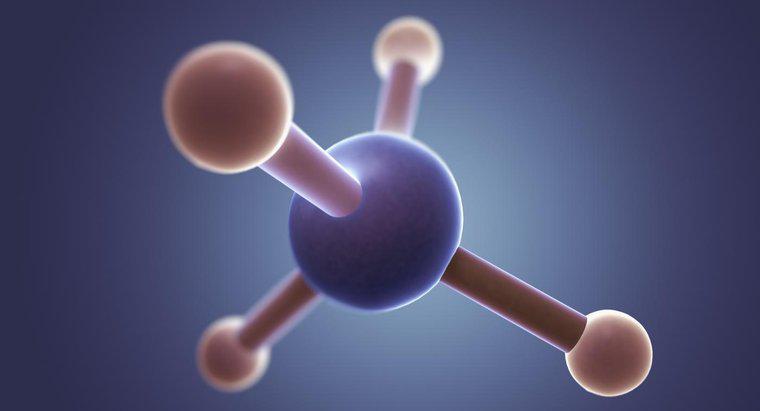
CF4, czyli tetrafluorometan, jest cząsteczką tetraedryczną. Jak wskazuje "tetra" część nazwy, cząsteczka ma cztery grupy elektronów związanych wokół centralnego atomu.
Podobnie jak w przypadku wielu wiązań elektronów, istnieje kilka części cząsteczki tetraedrycznej. Główną częścią cząsteczki jest atom, który zawsze znajduje się w centrum. Cztery grupy elektronów są rozmieszczone wokół atomu. Te elektrony nigdy nie są w samotnych parach i zawsze pozostają razem w równomiernym układzie wokół atomu, chociaż nie zawsze są one równe odległościom od siebie.
Ponieważ elektrony są bardziej przyciągane do fluoru niż do węgla, elektrony spędzają więcej czasu bliżej fluoru w modelu CF4. Elektrony są utrzymywane razem z wiązaniami kowalencyjnymi, a wiązania te ciągną się w kierunku fluoru i odciągają od węgla. Chociaż fluor i węgiel są w pewnym stopniu równe, fluor ma mocniejsze przyciąganie. Wzór chemiczny CF4 odzwierciedla większe przyciąganie elektronów do fluoru. Brak liczby z węglem oznacza, że elektrony nie są przyciągane do węgla, ale zamiast tego są odsuwane od niego.