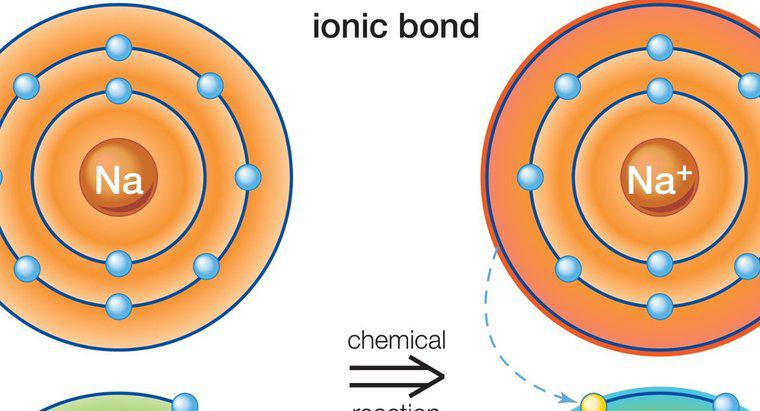
Związki jonowe to ciała stałe, mają wysokie temperatury topnienia, przewodzą prąd elektryczny, są twarde, ale kruche i powstają z wiązań jonowych między jednym metalem a jednym niemetalem. Wiązanie jonowe to wiązanie między dwoma pierwiastkami z przeciwnymi opłatami. Przeciwne ładunki przyciągają się nawzajem, tworząc silne wiązanie chemiczne.
Związki jonowe łatwo rozpuszczają się w polarnych rozpuszczalnikach, takich jak woda. Nie rozpuszczają się łatwo w niepolarnych rozpuszczalnikach, które obejmują eter i benzynę. Wynika to z tego, że związki jonowe mają tendencję do tworzenia cząsteczek polarnych, które rozpuszczają się w roztworach o podobnej polarności. Niepolarny rozpuszczalnik nie zapewnia wystarczającej energii do przerwania wiązania jonowego i rozpuszczenia krystalicznej struktury związku.
Właściwości przewodzące związków jonowych mają zastosowanie, gdy są rozpuszczone w roztworze jonowym lub gdy są stopione. Kiedy związki jonowe są stałe, są raczej izolatorami elektrycznymi niż przewodnikami. Dzieje się tak dlatego, że ładunki elektryczne nie mogą przechodzić przez ciasną strukturę sieci związku jonowego w jego stanie stałym.
Chlorek sodu, znany również jako sól kuchenna; chlorek potasu, który jest stosowany w medycynie i jako substytut soli; a korund, minerał, z którego składają się rubiny i szafiry, to dobrze znane związki jonowe. Wszystkie te związki tworzą struktury krystaliczne, inną wspólną cechę związków jonowych.