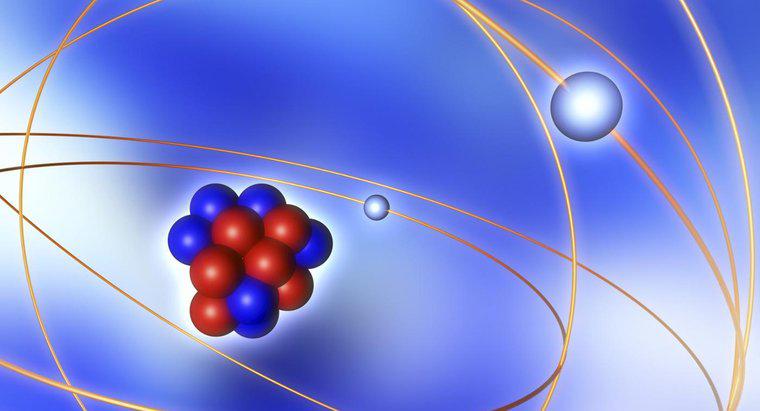
Jądro atomu zawiera neutrony i protony. Protony są naładowane dodatnio, a neutrony są neutralne. Elektrony, będąc częścią atomu, nie są częścią jądra.
Atomy są elektrycznie obojętne, co oznacza, że mają równą ilość ładunku ujemnego i dodatniego. Ładunek netto jądra atomu jest dodatni z powodu pozytywnych protonów. Aby temu przeciwdziałać, elektrony naładowane ujemnie krążą wokół jądra.
Neutralny atom ma taką samą liczbę protonów jak elektrony. W przeciwieństwie do protonów liczba neutronów w jądrze może być różna. Atom, który zawiera odpowiednią ilość protonów i elektronów, ale z inną liczbą neutronów w jądrze, nazywany jest izotopem.
Większość masy atomu znajduje się w jądrze. Elektrony są znacznie lżejsze niż protony i neutrony.
Nawet jeśli jądro zawiera większość masy atomu, jest bardzo małe w porównaniu z całkowitym rozmiarem atomu. Dzieje się tak dlatego, że protony i neutrony są ściśle ze sobą połączone dzięki sile nuklearnej. Bez tej siły nuklearnej pozytywne protony odpierałyby się wzajemnie, a jądro nie istniałoby. Jeśli siła jądrowa jest zbyt słaba, jądro rozpada się, powodując emisję radioaktywną.